2018年2月1日/医麦客 eMedClub/--对于高风险形式的急性淋巴细胞白血病(ALL)患者来说,诺华的CAR-T细胞产品tisagenlecleucel(CTL019)绝对称得上是具有里程碑意义的个性化治疗方法。今日,《新英格兰医学杂志》上公开发表了一项其最新的全球试验结果,表明该CAR-T疗法在儿童和年轻成人B细胞淋巴细胞白血病患者中持续显示出高耐用性以及完全缓解状态,并且治疗过程中发生的大多数副作用都是短暂且可逆的(CHOP(费城儿童医院)肿瘤学家更新关于CAR-T细胞治疗复发或难治性ALL的关键全球试验的分析)。

根据先前的研究结果,美国FDA已于2017年8月30日批准了tisagenlecleucel (CTL-019)上市,用于治疗儿童和年轻成人(2-25岁)的急性淋巴细胞白血病(ALL),商品名为Kymriah,是人类历史上批准的首款CAR-T疗法。
而此次公布的临床结果是由诺华公司发起的,在全球11个国家的25个中心进行的一项名为ELIANA的试验(ClinicalTrials.gov注册号为NCT02435849)。

众所周知,嵌合抗原受体T(CAR-T)细胞疗法是通过基因修饰患者的免疫细胞,使其能够找到并杀死白血病细胞。该方法是由宾夕法尼亚佩雷尔曼医学院的Carl June博士领导的一个团队开发的,作为该团队的共同合作单位,费城儿童医院(CHOP)是第一家在白血病儿童中使用该疗法的机构。
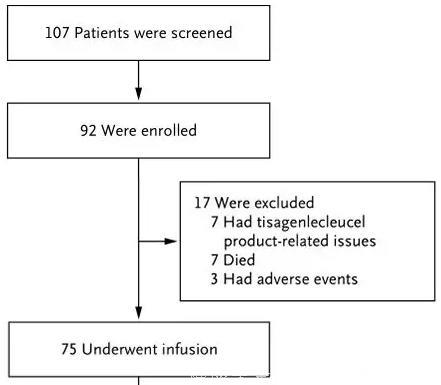
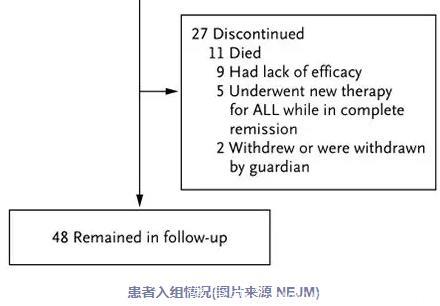
目前的研究包括对75例25岁以下的患者进行长期随访的安全性和有效性数据:

作为该论文的主要作者,费城儿童医院的儿科肿瘤学家Shannon L. Maude博士说:“这项扩大的、全球性的CAR-T细胞治疗研究为我们提供了进一步的证据,证明这种治疗方法对于所有其他治疗失败的年轻患者来说是非常意义重大的。我们的数据显示,CAR-T细胞治疗不仅可以实现长期持久的缓解和更长的生存期,而且这些个性化的细胞还可以在体内停留数月甚至数年,从而有效地发挥抗癌作用。”
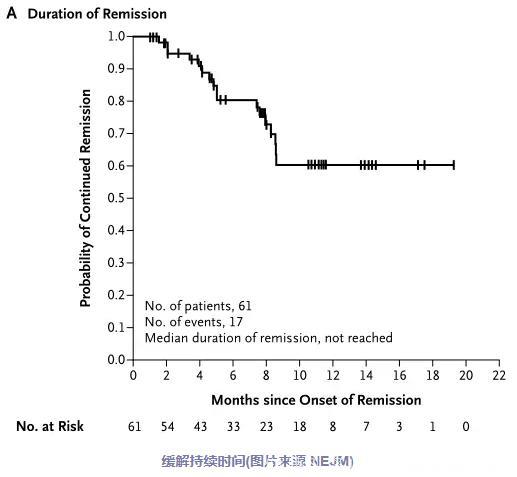
在这项试验中,75例儿童和年轻成人患者接受了tisagenlecleucel的输注并可进行疗效评估。61名患者(81%)对治疗有反应,并在3个月的随访后被定义为完全缓解,血细胞计数完全恢复。61例患者的无复发生存率在治疗6个月后为80%,12个月时为59%。所有75例患者中,6个月时的无事件生存率和总生存率分别为73%和90%,12个月时的无事件生存率和总生存率分别为50%和 76%。对此,论文作者表示,生存率是早期应答率持久的证据。因为在没有CAR-T细胞治疗的情况下,经历多次复发或难治性B细胞ALL患者的预后通常较差。
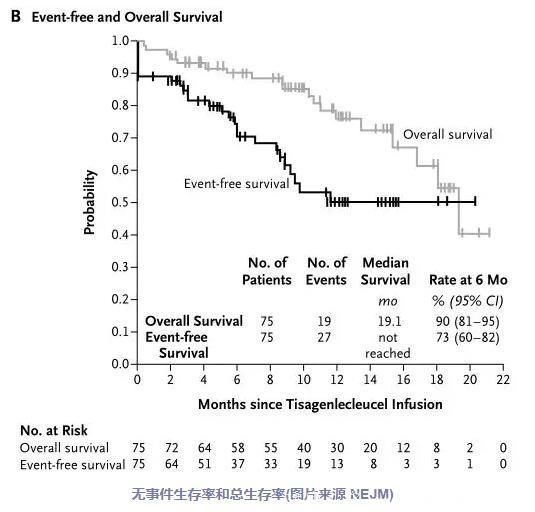
伴随着持久的反应,CAR-T细胞在患者血液中持续存在长达20个月,在本研究分析数据时的中位持续时间为168天,所有试验中的患者均只接受过CAR-T细胞的单次输注。
安全性方面,与CAR-T细胞治疗的早期研究一致,最常见的与治疗相关的副作用是CRS,75名中近一半的患者由于CRS进入了重症监护病房治疗,但不良事件都是短暂且可逆的。(73%的患者出现了疑似与tisagenlecleucel相关的3级或4级不良事件。77%的患者出现了细胞因子释放综合征,其中48%接受了托珠单抗治疗。40%的患者出现了神经系统事件,采用支持性疗法对这些事件进行了管理,没有脑水肿的报告)
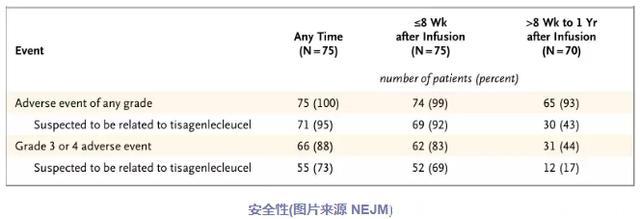
“在这项全球性研究中,一个更具挑战性的问题是,是我们能否处理CAR-T细胞疗法的严重副作用?”
作为本次2期临床试验的首席研究员,宾夕法尼亚大学佩雷尔曼医学院的儿科教授、CHOP癌症免疫治疗前沿项目主任Stephan A. Grupp博士表示:“我们的一些病人病症特别严重,但是我们发现大多数毒性反应可能是短暂的和可逆的,病人仍可能获得持久的、完全的缓解,而这对于高风险的、直到现在幸存机会都很小的儿童患者来说,是一个相当惊人的转折。”
目前,研究小组正在不断的进行临床试验,以期最大限度的减轻CAR-T治疗相关的严重的副作用并克服复发难题。
参考出处:
https://www.prnewswire.com/news-releases/t-cell-therapy-shows-persistent-benefits-in-young-leukemia-patients-300591426.html
DOI: 10.1056/NEJMoa1709866
医麦客 丨出品
中国生物医药产业新媒体
转载请联系:[email protected]
☟ 阅读原文 报名参会
申明:文中资讯内容和事件评述仅代表作者观点,如果出现与事实不符或版权侵犯的内容,请速与医麦客平台联系,我们会尽快做出处理,欢迎更多读者朋友关注并给出指导建议。