本文转载自微信公众号“药明康德”
丙肝患者福音!病毒学检测无论是哪一种基因型的丙肝病毒(HCV)感染,都将迎来新的治疗选择。
通吃丙肝病毒
近日,美国FDA刚刚批准了Gilead Sciences公司产品新药Vosevi(sofosbuvir 400 mg/velpatasvir 100 mg/voxilaprevir 100 mg)用于治疗慢性丙肝病毒(HCV)成年患者,他们无肝硬化(cirrhosis)症状或仅患有轻度肝硬化。适用患者群体为先前用含有NS5A抑制剂方案治疗失败的基因型1-6的成年患者,以及先前使用含有sofsbuvir但无NS5A抑制剂方案失败的基因型1a或3的成年患者。
Vosevi是一种含三种固定剂量成分的组合药片,其中两种为先前获批药物sofosbuvir和velpatasvir,以及一个新药物化学分子voxilaprevir(泛基因型NS3蛋白酶抑制剂)。针对先前已经接受过直接抗病毒药物sofosbuvir或NS5A抑制剂治疗的患者,Vosevi是首个获得FDA批准的治疗方案。

丙肝的危害
丙型肝炎是一类引起肝脏炎症的病毒性疾病,可导致肝功能下降或肝功能衰竭。据世界卫生组织(WHO)统计,中国约有1000万人口是慢性HCV感染者,其中250万人急需治疗。一些患有多年慢性HCV感染的患者可能会出现黄疸(黄色眼睛或皮肤)症状,并有出血、腹部积液、感染、肝癌甚至死亡等并发症。目前,至少发现了六种不同基因型的HCV菌株,它们是遗传定义上不同的病毒类群。
疗效数据参考
研究人员在两个3期临床试验(POLARIS-1和POLARIS-4)中评估了Vosevi的安全性和有效性,其中涉及约750名没有肝硬化症状或有轻度肝硬化的成年患者。
与安慰剂组比较,第一项试验评估12周疗程的Vosevi治疗HCV基因型1感染患者,他们先前接受NS5A抑制剂药物治疗失败。HCV基因型2、3、4、5或6的患者也都接受了Vosevi。在第二项临床试验中,与先前获批药物sofosbuvir + velpatasvir治疗方案相比较,评估了12周疗程的Vosevi治疗基因型1、2或3的成年患者,他们曾使用sofosbuvir(但非NS5A抑制剂)治疗失败。
两项试验结果表明,96-97%接受Vosevi的患者在完成治疗后12周没有在血液中检测到病毒,表明患者的病毒感染已经被治愈。
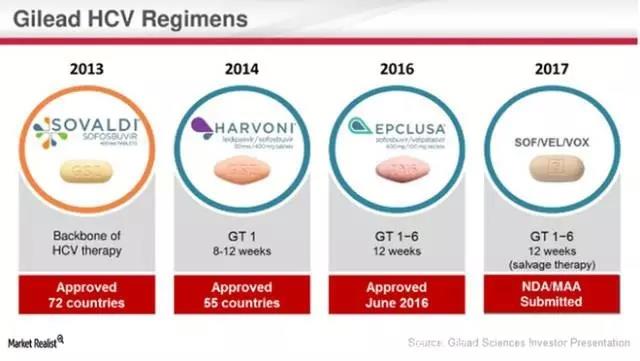
▲近年来Gilead Sciences公司获得批准的HCV新药组合(图片来源:Market Realist)
Vosevi是Gilead基于sofosbuvir的直接作用的抗病毒(DAA)治疗产品组合中最新的单片药物,为HCV患者人群提供了方便、短期的一日一次的单片剂治疗方案。
FDA药物评估与研究中心下属的抗菌药物办公室主任Edward Cox博士说道:“直接作用的抗病毒(DAA)药物往往可以防止病毒繁殖并常常治愈HCV。但有些患者不能从中获益,Vosevi为这些未能成功获得治疗的HCV患者提供了治疗选择。”
参考资料:
[1] FDA approves Vosevi for Hepatitis C
[2] Gilead Sciences官方网站
[3] WHO官网
本文由药明康德团队打造,系原创作品,转载需申请授权,并请注明出处“e药环球”。
更多内容请关注药明康德传媒网站:http://www.wuximediaglobal.com/










