近日,美国食品药品监督管理局(FDA)批准礼来公司的CDK4/6抑制剂Abemaciclib(商品名VERZENIO)联合芳香化酶抑制剂,用于绝经后激素受体(HR)阳性、且人类表皮生长因子受体2(HER2)阴性的转移性乳腺癌一线治疗。
什么是激素受体阳性乳腺癌?乳腺的正常工作有赖于多种激素的协调作用,尤其是雌激素和孕激素,而这些激素必须与细胞内的特异性蛋白质相结合才能发挥作用,这些特异性的蛋白质叫做雌激素受体(ER)和孕激素受体(PR)。
当细胞发生癌变时,仍有可以正常发挥作用的雌、孕激素受体,癌细胞的生长也同样受雌、孕激素的调控,这类肿瘤称为激素依赖性肿瘤。大约60%的乳腺癌都是激素依赖性肿瘤。
当乳腺癌患者体内的雌/孕激素与癌细胞的雌/孕激素受体结合时,就如同一把钥匙开一把锁一样,打开了癌细胞生长、分裂的开关。如果癌细胞ER/PR表达阳性,则肿瘤细胞的生长和增殖受雌、孕激素的调控,此时内分泌治疗有效,这类患者称为“激素受体阳性乳腺癌”。
什么是“HER2阴性乳腺癌”和“转移性乳腺癌”?驱动乳腺癌生长的三种受体分别是雌激素受体(ER)、孕激素受体(PR)及人表皮生长因子受体2(HER-2)。乳腺癌患者在确诊时会进行这三种受体的检测,根据受体以及基因突变情况将乳腺癌分为管腔Luminal A、Luminal B、HER2阳性、三阴乳腺癌四种类型。HER2阴性乳腺癌,就是指不存在HER2过表达的乳腺癌类型。
转移性乳腺癌是乳腺癌最晚期的阶段。在这一阶段,癌细胞已扩散到乳房以外的其他部位,最常见的是肺部、脑部和骨骼。
过去三十年里,尽管相关治疗方案有所增加,但目前尚没有能够治愈转移性乳腺癌患者的药物。在确诊后,存活期超过5年的患者仅有26.9%。因此,治疗的主要目的是尽可能延缓疾病进展,改善或至少维持患者的生活质量。
Abemaciclib疗效如何?此次FDA批准Abemaciclib联合芳香化酶抑制剂用于绝经后HR+/HER2-的转移性乳腺癌,是基于该药物的MONARCH 3 III期试验数据。
MONARCH 3是一项随机双盲、安慰剂对照、多中心开放性III期试验,研究共入组493例HR+/HER2-的绝经后晚期、既往未接受过挽救治疗的乳腺癌患者,以2:1随机分配接受Abemaciclib+阿那曲唑或来曲唑(Abemaciclib组)和安慰剂+阿那曲唑或来曲唑(安慰剂组)治疗,旨在评估两者的疗效和安全性。主要研究终点为无进展生存期(PFS),次要研究终点包括:总生存期(OS)、客观缓解率(ORR)和安全性。
研究结果显示,Abemaciclib组PFS达到28.2个月,安慰剂组PFS 14.8个月,前者显著延长PFS 13.4个月,将近延长一倍!Abemaciclib组的平均反应持续时间为27.4个月,而对照组为17.5个月。Abemaciclib组ORR达到55.4%,安慰剂组ORR 40.2%,提高了15.2%。各个亚组患者均观察到Abemaciclib的疗效。Abemaciclib组联合方案耐受性较好,常见的AE包括腹泻,中性粒细胞减少和乏力等。
推荐Abemaciclib起始剂量与芳香酶抑制剂联合应用,每天两次,每次150毫克。
Abemaciclib是个什么药?它为何有效?Abemaciclib是一种CDK4/6抑制剂,它是全球获批的第3款CDK4/6抑制剂,其他两款分别是辉瑞的Palbociclib(帕博西林),诺华的Ribociclib(瑞博西林)。
周期蛋白依赖性激酶(CDK)4/6 是细胞周期的关键调节因子,通过与cyclin D形成复合物,磷酸化Rb,释放E2F,触发细胞周期从DNA合成前期(G1期)进入到 DNA 复制期(S1期),从而促进进肿瘤的生长。
在ER+乳腺癌中,CDK4/6-cyclinD-Rb通路非常重要,且是ER信号的关键下游靶标。因此,CDK4/6抑制剂阻断了CDK4/6激酶的活性,恢复细胞周期控制,阻断肿瘤细胞增殖,也就抑制了乳腺癌细胞的生长。因此,Abemaciclib有望能控制乳腺癌的进展,改善病情。
2017年9月,FDA批准Abemaciclib联合氟维司群用于内分泌治疗后HR+/HER2-晚期乳腺癌伴疾病进展的患者,以及单药用于接受过内分泌治疗和化疗的HR+/ HER2-晚期乳腺癌患者。通俗的讲,获批的是二线治疗方案。
此项获批是依据一项III期临床试验结果,入组经内分泌治疗后疾病进展的HR+/HER2-晚期乳腺癌患者669例,随机分到Abemaciclib+氟维司群联合组和氟维司群单药组。
结果显示,联合组的中位PFS为16.4个月,而单药组患者中位PFS为9.3个月。Abemaciclib使患者的PFS有显著改善,因此获批作为经内分泌治疗后进展的HR+/HER2-乳腺癌二线治疗。
Abemaciclib最常见的不良反应为腹泻(90.2%)、疲劳(65.2%)、恶心(64.4%)、食欲降低(45.5%)、腹痛(38.6%)、白细胞减少(27.4%)和嗜中性粒细胞减少(22.3%)。
3级不良反应中,腹泻占19.7%,疲劳为12.9%,恶心为4.5%,食欲下降为3.0%,腹痛为2.3%。唯一一个4级不良反应为嗜中性粒细胞减少症,4.6%的患者出现嗜中性粒细胞减少症。
这项批准是一个重要的里程碑,因为它表明Abemaciclib联合芳香化酶抑制剂可显着减少HR+/HER2-转移性乳腺癌的肿瘤大小和延缓疾病进展!不光在二线治疗中见到效果,一线治疗也不遑多让,对于凶险异常的转移性乳腺癌患者而言是一件值得高兴的事情。
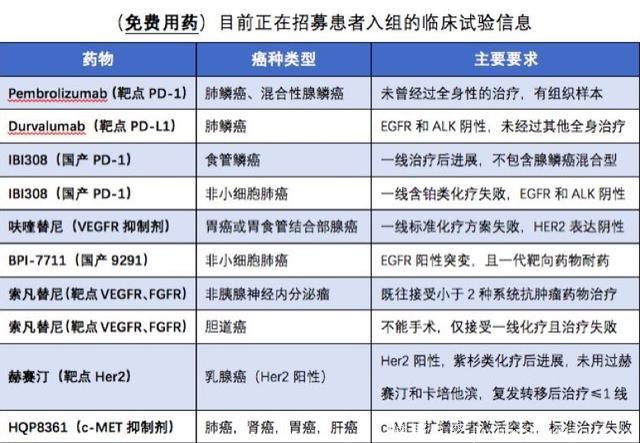
如您的肿瘤类型、治疗经历符合下表要求,点击下方“了解更多”,即可登记申请参加临床试验。