导读
随着时间的推移,膀胱癌的治疗也在不断发展。自第一代免疫治疗出现以来,减毒细菌卡介苗疫苗一直被视为非肌层浸润性膀胱癌的标准治疗手段。现代免疫治疗主要集中于免疫检查点蛋白抑制剂,而PD-1/PD-L1和CTLA-4检查点靶点在膀胱癌的治疗中也越来越受关注。
膀胱癌是全球第九大最常见的癌症,每年约影响43万人,导致16.5万人死亡。膀胱癌的最大危险因素是吸烟,全球发病率与吸烟率相对应。过去的20年中,研究人员投入了大量的时间,精力和物力用于膀胱癌的研究,但是其总发生率和死亡率并未明显改善。现代膀胱癌治疗手段包括手术,化疗,放疗和免疫治疗。
恶性细胞与正常细胞具有抗原性差异,它们已经发展了许多免疫逃逸机制。癌细胞可以下调细胞表面上的肿瘤抗原表达,从而隐蔽自身,或在细胞表面表达其它蛋白质,诱导免疫细胞失活;此外,癌细胞还可以诱导肿瘤微环境释放细胞因子,如TGF-β,抑制免疫应答,促进肿瘤细胞增殖和存活。免疫治疗的潜能促进了肿瘤免疫学的发展,目前最具前景的研究是应用单克隆抗体阻断有效免疫应答的负共信号分子。这些“检查点”抑制剂可以重新激活T细胞介导的抗肿瘤活性。
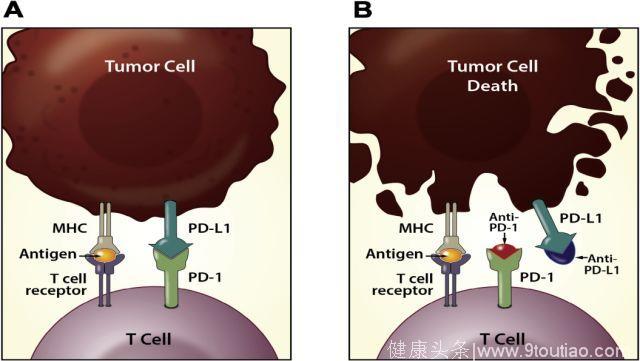
三种主要的检查点靶点为PD-1,PD-L1和CTLA-4,它们一直是膀胱癌治疗研究的重点。已有研究证实,PD-L1表达的水平与膀胱癌的严重程度和结果相关。PD-L1高表达的肿瘤可能为高级肿瘤,并且器官限制性疾病患者术后复发率很高,存活较差。此外,肿瘤细胞PD-L1表达于BCG治疗耐药性增强有关。
然而,最新研究发现,NMIBC和肌层浸润性膀胱癌(MIBC)的PD-L1表达并没有差异,肿瘤浸润的单核细胞表面PD-L1的表达预示着发生转移并接受后续化疗治疗的患者具有较长的OS,这可能是由于此类细胞的抗肿瘤特异性。高突变负荷的肿瘤,如膀胱癌,能够引发更强的T细胞介导的抗肿瘤免疫反应,可能更获益于面积检查点抑制剂。
Atezolizumab
Atezolizumab是首个获FDA批准用于膀胱癌新靶向治疗的PD-L1抑制剂。 II期队列2 IMvigor 210试验共纳入了310名不能手术,且在接受铂类药物化疗后病情进一步恶化的局部晚期或转移性尿路上皮癌患者(年龄≥18岁)。患者每3周或21天静脉注射 atezolizumab 1200mg。研究者观察的指标包括客观应答率、应答持续时间、总生存期和无进展生存期,此外还探究了药物的安全性,以及PD-L1表达阳性或阴性患者中atezolizumab的疗效差异。
中位随访1.5年后,atezolizumab(1200 mg IV q3w)治疗的所有患者的客观应答率(ORR)为16%,PD-L1表达的肿瘤浸润性免疫细胞(IC)患者的ORR为28%。最常见的不良反应是疲劳和恶心,3/4级不良事件发生率为16%。目前,肾细胞癌,黑色素瘤以及三阴性乳腺癌等仍在研究阶段。
Nivolumab
Nivolumab是一种直接靶向PD-1的单克隆抗体,是世界上第一个获批的PD-1抑制剂,2014年7月在日本获批上市,用于无法切除的黑色素瘤治疗。目前在美国获批用于转移性黑色素瘤,NSCLC,肾细胞癌,霍奇金淋巴瘤,头颈鳞状细胞癌以及一线铂类化疗一年内疾病进展的局部晚期转移性尿路上皮癌患者的治疗。2015年,nivolumab在欧洲获批用于晚期黑色素瘤和非小细胞肺癌治疗。2016年4月获批用于肾细胞癌治疗。
2012年公布的首个临床试验结果显示,晚期实体恶性肿瘤(N=296),如黑色素瘤,NSCLC,前列腺癌,肾细胞癌和结直肠癌患者应答率为18%~28%不等,65%的应答持续一年或一年以上。一项非随机,I/II期研究纳入了78名转移性尿路上皮癌患者,患者每两周静脉注射3mg/kg nivolumab。结果表明,肿瘤细胞表面PD-L1表达≥1% 的患者ORR为24%,而PD-L1表达<1%的患者ORR为26%,整个受试人群总生存期为9.7个月。
一项单臂,开放标签研究纳入了265名曾治疗的转移性尿路上皮癌患者,每两周静脉注射3 mg/kg治疗。随访7个月后,总人群ORR为19.6%,低或无PD-L1表达(<1%)肿瘤患者ORR为16.1%,PD-L1表达≥5%的肿瘤患者ORR为28%。中位PFS为2.0个月,中位OS为8.7个月。18%的患者发生3/4级不良事件,疲劳和腹泻各占2%,1%的患者发生5级不良事件。手术后膀胱或上尿路癌患者nivolumab与安慰剂的III期对照研究正在进行中。
目前正在进行nivolumab联合ipilimumab治疗不同肿瘤的大量研究。PD-1主要在T细胞活化的效应阶段发挥作用,PD-1/PD-L1相互作用主要发生于外周组织和器官。CTLA-4由Treg细胞和记忆性CD4+细胞表达,在淋巴组织T细胞早期激活过程中起作用。CheckMate 032试验探究了nivolumab联合ipilimumab治疗的疗效:队列A(n=26)nivolumab(1 mg/kg)联合ipilimumab(3mg/kg),队列B(n=104)nivolumab (3mg/kg)联用ipilimumab(1mg/kg)。
结果表明,相对于较低剂量ipilimumab组合,较高剂量组应答率较高。两组总生存相似:队列A=10.2个月(95% CI, 4.5-NR);队列B=7.3(95% CI, 5.6-11.4个月)。两组患者的中位无进展生存期均少于5个月。不良事件与在既往其它肿瘤中观察到的治疗一致。另外两项关于nivolumab和ipilimumab联用治疗膀胱癌的研究正在进行中。
参考文献:
[1]Topalian SL, Hodi FS, Brahmer JR, Gettinger SN, Smith DC, McDermott DF, et al. Safety, activity, and immune correlates of anti-PD-1 antibody in cancer. N Engl J Med 2012;366:2443–54.
[2]Sharma P, Callahan MK, Bono P, Kim J, Spiliopoulou P, Calvo E, et al. Nivolumab monotherapy in recurrent metastatic urothelial carcinoma (CheckMate 032): a multicentre, open-label, two-stage, multi-arm, phase 1/2 trial. Lancet Oncol 2016;17:1590–8.
全方位盘点丨肿瘤免疫治疗的靶向通路








