摘要
abstract
2018年1月药品注册申请继续稳定增加再有三个CAR-T疗法药物进入CDE2018年首个中药1类新药知母皂苷BII获CDE承办 甲苯磺酸索拉非尼片以及马来酸阿法替尼片均有首仿申请阿斯利康重磅哮喘新药Tezepelumab注射液申请国内临床4个1类新药临床申请获批
承办情况
据米内网MED中国药品审评数据库2.0统计,2018年1月CDE共承办药品注册申请514个。从总体上看,药品注册申请增长稳定。
图1:2017年8月-2018年1月CDE承办药品注册申请情况(按受理号计)
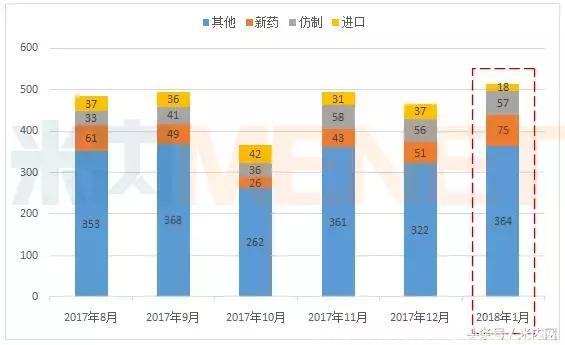
(来源:米内网MED中国药品审评数据库2.0,下同)
1月有19个一致性评价申请进入CDE,涉及13个品种。值得注意的是,恒瑞医药的卡培他滨片目前已离开一致性评价新报任务序列。
表1:2018年1月仿制药一致性评价受理情况
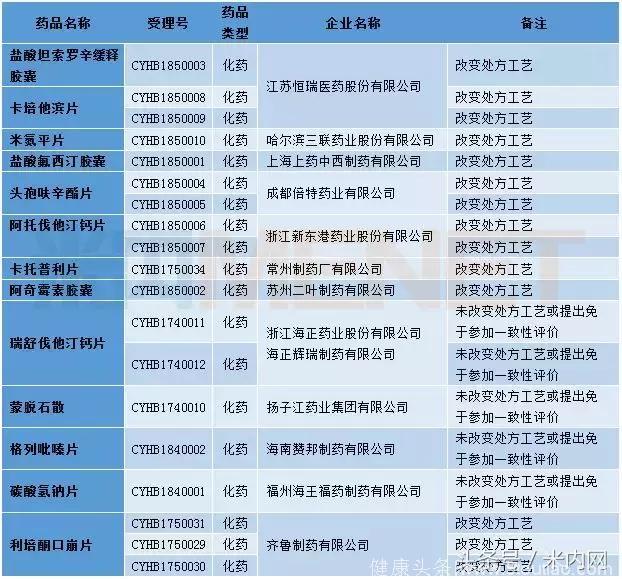
国内新药承办
1月新药申请有75个,其中属于1类新药的申请有38个,涉及21个通用名。上海优卡迪生物、上海明聚生物以及博生吉安科的CAR-T疗法药物进入CDE,截至目前已有7个CAR-T疗法药物在CDE进行审评。此外还有两个糖尿病新靶点药物获CDE承办,分别是江苏万邦的SGLT-2抑制剂万格列净以及银诺医药的GLP-1激动剂苏帕鲁肽注射液。知母皂苷BII成为2018年首个进入CDE的中药1类新药。
表2:2018年1月1类新药承办情况
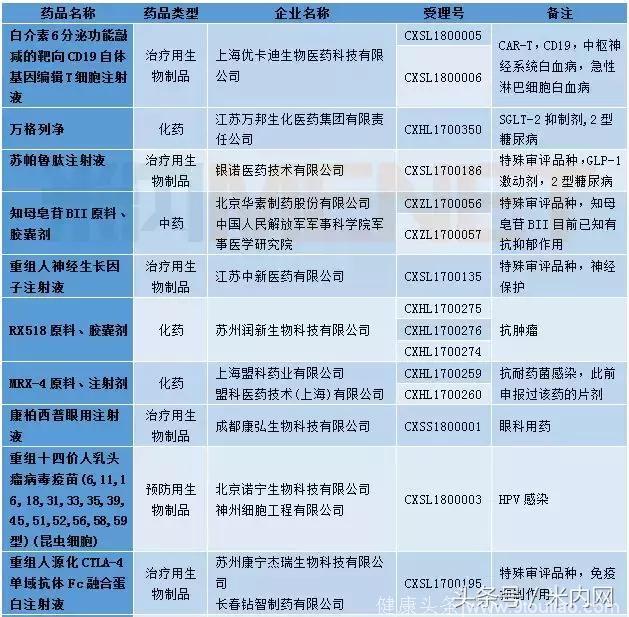
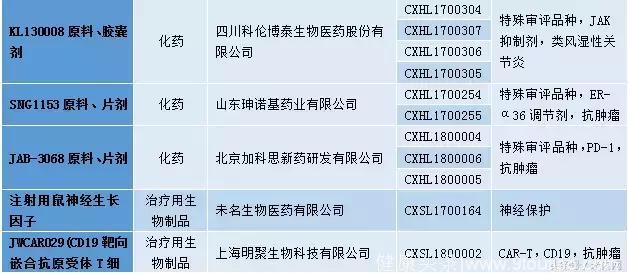
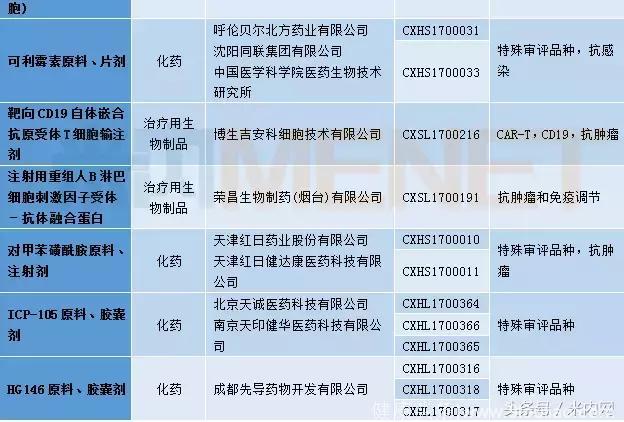
国内仿制药承办
1月CDE共承办仿制申请57个,属于3类的申请有26个,涉及21个品种。属于4类的申请有31个,涉及23个品种。
在1月获得CDE承办的仿制申请中有15个品种目前为国内独家品种。甲苯磺酸索拉非尼片以及马来酸阿法替尼片均有首仿申请。
阿仑膦酸钠片、苯磺酸氨氯地平片以及盐酸氨溴索注射液等品种已有注册批文较多,有同质化迹象。
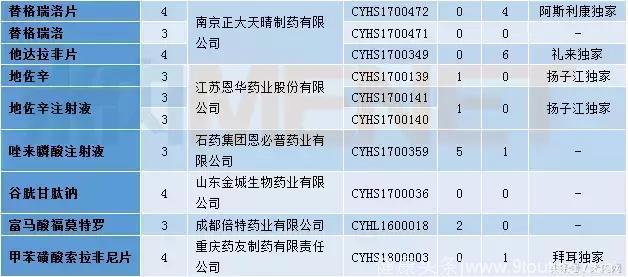
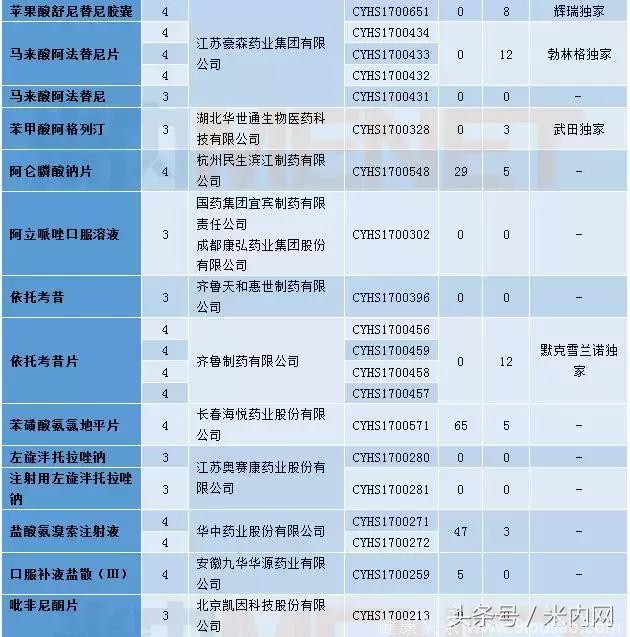
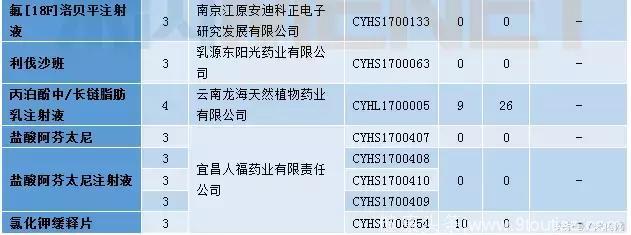
表3:2018年1月仿制申请承办情况
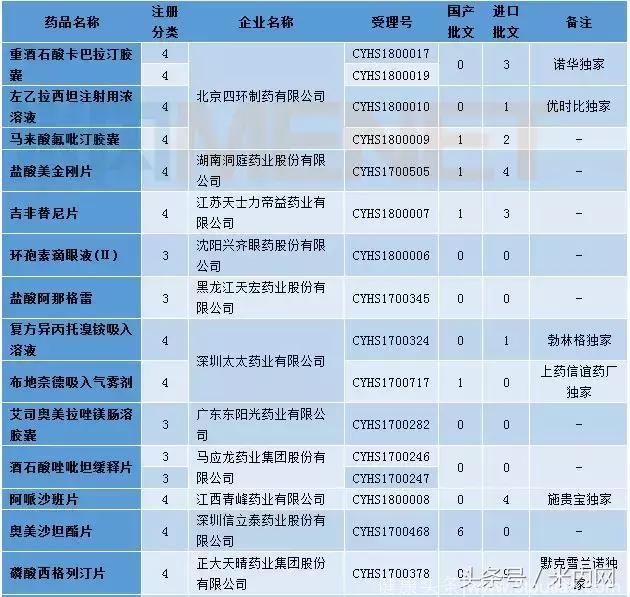

进口申请承办
1月份有3个品种首次获CDE承办。注射用盐酸替拉凡星是一款脂糖肽类抗生素,用于治疗革兰阳性菌造成的复杂性皮肤和皮肤软组织感染。Rogaratinib是一款FGFR抑制剂,拟用于肺癌治疗。Tezepelumab注射液是首个TSLP抗体哮喘新药,国外二期临床试验显示积极结果。
表4:2018年1月首次获CDE承办的进口品种

审批情况
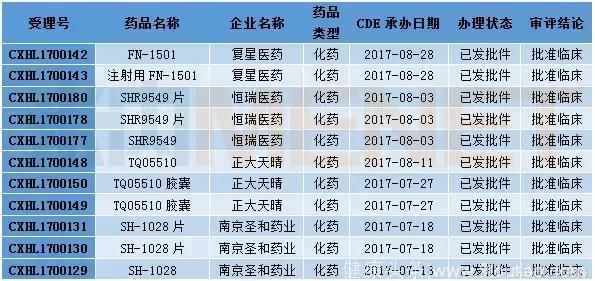
2018年1月有多个1类新药获批临床,均为2017年CDE承办申请。
表5:2018年1月1类新药获批情况