今天是2017年10月4日
农历八月十五
医麦客:祝大家中秋节快乐
2017年10月4日/医麦客 eMedClub/--来自美国西雅图的消息,10月2日,纳斯达克上市公司Atossa Genetics宣布即将推出针对实体瘤乳腺癌的CAR-T疗法。
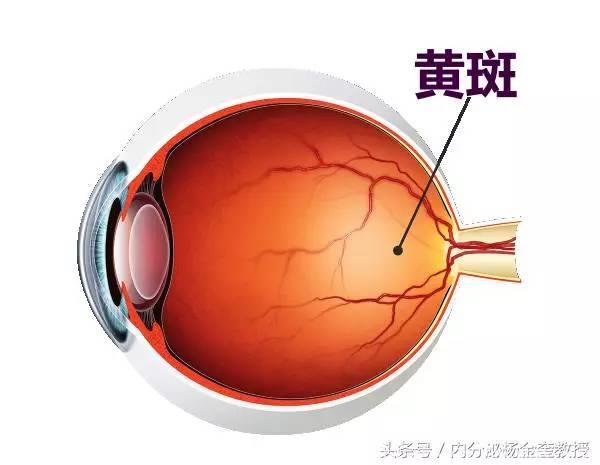
Atossa Genetics是一家为乳腺癌和其他乳腺疾病开发新型治疗和递送方法的临床阶段制药公司,公司CAR-T计划是使用其独有的微导管技术将CAR-T细胞递送至乳腺导管,用于针对乳腺癌潜在的靶向治疗。
1 独有的微导管TRAP CAR-T技术
Atossa公司的新颖方法是使用其独有的微导管技术,通过潜在的毛细血管(简称TRAP)传递已被遗传修饰的针对侵袭性乳腺癌细胞的T细胞。
乳腺癌临床试验中乳头状毛细血管(TRAP)的递送方式经过证明,结论是:“细胞毒性药物可以安全地施用到具有最小毒性的乳腺导管中”。该处Atossa公司公司还引用了来自中国科学家的研究结果。(Zhang B,et al。Chin J Cancer Res.2004 Oct; 26(5): 579-87; www.ncbi.nlm.nih.gov/pubmed/25400424)。
将T细胞从患者中取出并进行修饰,使得它们表达对患者特定乳腺癌特异性的受体。然后,可以使用微导管将T细胞导入乳房的天然导管中,从而识别并杀死癌细胞。
Atossa认为这种方法有几个潜在的优点:
通过限制T细胞的全身暴露以降低细胞毒性;
通过将T细胞与正在经历恶性转化的导管上皮细胞直接接触来提高CAR-T细胞治疗的功效;
通过迁移癌细胞所采取的相同途径的CAR-T细胞的淋巴迁移,潜在地将其细胞毒作用扩展到局部淋巴系统,这可能会限制肿瘤细胞传播。

Steven Quay博士
Atossa首席执行官Steven Quay博士说:“CAR-T细胞疗法已经表现出针对其他形式的癌症,比如恶性实体瘤,这让我们深受鼓舞。我们相信独有的TRAP技术可以为提供CAR-T提供一种更安全,有效的方法。”
TRAP CAR-T可以称为乳腺癌适应性T细胞治疗的新方法,这为乳腺癌的治疗提供新的策略,并且可能特别适合致命性乳腺癌,例如三阴乳腺癌。目前TRAP CAR-T技术正在申报国际专利,我们计划通过与世界各地领先的科学家,机构和组织继续开展合作研发,使Atossa的技术和TRAP的专利授权给癌症免疫学和T细胞生物学专家。
Quay博士补充道:“动物和人类的多项研究表明,TRAP,导管内途径可以传递一些治疗药物,同样适用于CAR-T细胞。”
提示:Atossa的方法在研发阶段,尚未得到FDA或任何其他监管机构的上市批准。在商业化之前,需要进行临床前研究和证明安全性和有效性以及其他方面的临床研究以及监管批准。
2 独有的微导管TRAP CAR-T技术

Atossa Genetics是一家临床阶段的制药公司,旨在开发新型治疗和递送方法来治疗乳腺癌和其他乳腺疾病。他们的微导管TRAP专利技术是通过乳头将药物直接传递到癌症的位置。这种递送方法的目的是增加药物到达目标区域的量,同时减少通过血液递送药物引起的副作用。
2015年12月份,公司宣布FDA已接受其治疗原位管癌或乳癌药物Fulvestrant的IND申请,正在准备展开开放性、非随机的2期临床研究,评估药代与安全性。Fulvestrant利用Actossa专利性微导管技术于患者病灶处滴注。
3 实体瘤CAR-T疗法面临的挑战
脱靶导致的安全性
不同于CD19仅表达于B细胞,实体瘤相瘤抗原往往不仅表达于肿瘤组织,在正常组可有低水平的表达,部分抗原甚至还有维持常生理功能的作用。因此,尽管现行CAR-T疗采用了阶梯式剂量爬升的输注方式,尽可能控制不良事件(adverse event,AE)的发生,但不良反应依然存在,其中最为突出的是脱靶效应(on-targ mor effects)。CAR-T细胞在清除表达相应肿瘤细胞同时,也可能攻击表达相同抗原的组织。
肿瘤特异性靶点的选择
靶点的选择是实体肿瘤CAR-T治疗的另外一个挑战。B细胞血液恶性肿瘤中CD19的表达几100%,然而异质性是实体肿瘤更为突出的特点。这也意味着即使是同一位患者同一个部位的肿瘤都可能表达不一样的肿瘤相关性抗原。如果只用一种单靶点的CAR-T细胞治肿瘤,那么理论上实体瘤高度异质性的特点必然会导致复发或无法根除。
CAR-T细胞的体内归巢与活化维持
将细胞归巢至肿瘤局部并且活化增殖是CAR-T细胞治疗起效的关键步骤。只有从外周血迁移至肿瘤部位的CAR-T细胞才有机会杀伤肿瘤。因此,有学者正在通过动物模型研究试图改变CAR-T本身的一些特性来增强细胞迁移至肿瘤的能力和效率。当然,CAR-T修饰性研究需要谨慎地开展大量安全性评估。
4 实体瘤CAR-T疗法的近期进展盘点
胰腺癌:宾大与诺华合作的meso-CAR T
在2015年美国临床肿瘤学会年会(ASCO)上,诺华和宾大公布了公布了他们合作开发的CAR-T药物CARTmeso(原名MesoCART),这是CAR T细胞首次在实体肿瘤—胰腺癌治疗上的突破,这项研究克服了实体瘤的第一个难关。
费城宾夕法尼亚大学的研究者们成功的制造了抵抗胰腺癌的适合的CAR T-细胞,并输入给6位有难治性疾病的患者,成功的使其中一位患者的一些转移灶消失了。4位患者发生了疾病进展,2位疾病稳定,分别持续3.7个月和5.3个月。研究还对4位患者的肿瘤代谢活性进行了观察。发现特化适应的T细胞,即 CARTmeso细胞(针对特异性抗原Mesothelin),可转移至患者的肿瘤位点。
该研究的主导者、宾夕法尼亚大学的医学副教授Gregory L. Beatty, MD, PhD表示,制作针对胰腺癌的CARTmeso细胞是可行和安全的。临床放疗等治疗虽然具有抗肿瘤活性,但是都很短暂。”
他说道,光有CAR技术是不够的,需要联合治疗以加强CARTmeso细胞的有效性及持续时间。研究人员发现几乎所有胰腺癌组织都过度表达间皮素(mesothelin),一种间皮细胞上常见的膜结合型蛋白。在此基础上,Beatty医生和其同事研发出第二代CAR—间皮素特异性嵌合抗原受体(CARTmeso)。
CARTmeso是诺华针对实体瘤推出的第一个产品,靶点间皮素是一种细胞表面的糖蛋白,表达于正常胸膜、心包和腹膜的间皮细胞上,高表达于多种肿瘤组织,比如胰腺癌、卵巢癌、乳腺癌、子宫内膜癌等。尽管公布的一期临床试验初步结果多少有些让人失望,但是这也是CAR T细胞首次在实体肿瘤—胰腺癌治疗上的突破。
胰腺癌:Celyad公司的NKR-2-CAR T
比利时的Celyad公司早前宣布其创新CAR-T NKR-2疗法在实体瘤中疗效的THINK临床1b 期试验招募到了第一名胰腺癌患者。
CAR-T NKR-2疗法也是一种CAR-T细胞疗法,但是与通常的CAR-T细胞疗法不同的是这些T细胞中表达的CAR不含有识别肿瘤表面抗原的抗体片段,而是包含着完整的人类NKG2D (Natural Killer Group 2D) 受体。NKG2D受体的配体在正常细胞中不表达或者表达量非常少,但是当细胞受到感染或者发生癌变时,这些配体的表达量会大幅度上升。CAR-T NKR-2细胞中表达的CAR将NKG2D受体与CD3ζ融合,导致当NKG2D受体与它的配体结合时会激活T细胞。
由于NKG2D受体识别的配体种类广泛,CAR-T NKR-2细胞疗法的安全性是一个需要验证的重要问题。Celyad公司去年结束的临床I期试验结果表明CAR-T NKR-2细胞疗法在治疗AML和MM患者时表现出良好的安全性和耐受性。
2017年3月,医麦客报道了Celyad宣布FDA批准其在美国开展“THINK”临床试验。这项名为“THINK”的NKR-2 CAR-T临床试验主要包含7种适应症:5种实体瘤(结直肠癌、卵巢癌、膀胱癌、三阴性乳腺癌以及胰腺癌)和2种恶性血液瘤(急性髓系白血病以及多发性骨髓瘤)。
胰腺癌:Bellicum公司的PSCA-CAR T
2017年2月,Bellicum Pharmaceuticals公司旗下CAR-T细胞疗法BPX-601已经进入I期临床治疗,目前为止,已有四名患者参加了BPX-601试验,临床招募工作正在继续。BPX-601疗法CAR序列针对的是前列腺干细胞抗原(PSCA)。
前列腺干细胞抗原(PSCA)是由人体自然产生的一种蛋白质编码基因,研究发现它确实与胰腺癌有关系。该试验的主要研究者Carlos Becerra博士说:“这是一种在前列腺癌中最初被鉴定为肿瘤抗原的细胞表面上发现的一种蛋白质,但随后的研究显示出PSCA在其他癌症包括胰腺癌的上调。实际上,60%到80%的胰腺癌都表达PSCA。
参与者必须是具有不可切除胰腺癌的成年人,其肿瘤必须对PSCA的表达测试为阳性。患者可能在手术后或化疗或治疗期间经历疾病进展,或者他们可能拒绝了标准治疗。但是他们必须具有足够的器官功能和超过12周的预期寿命,作为结果评估的一部分,将会对患者进行长达两年的随访。
这项名为“BP-012”的I期临床试验(ClinicalTrail.org 注册号:NCT02744287)在位于达拉斯的贝勒大学医学中心进行,是一项开放的非随机性剂量研究试验,主要是为了在30名不可手术切除的胰腺癌患者身上评估BPX-601联合Rimiducid治疗的安全性以及有效性(由Bellicum开发的Rimiducid旨在触发患者BPX-601患者的T细胞活化和增殖。它有助于控制治疗的活动和效力,是由人为施用于患者的,从而成为了治疗性T细胞免疫活性的一套“开关”)。试验将获得BPX-601的安全使用剂量、Rimiducid的安全注射剂量以及单次Rimiducid注射后CAR-T细胞随着时间推移的持续状态。
胶质母细胞瘤:宾大与诺华合作的EGFRvIII-CAR T
宾夕法尼亚大学和诺华医学研究所合作开发了靶向EGFRvIII的自体CAR-T治疗方式。在最新的一项临床试验中(NCT02209376),基因改造后的“hunter”T细胞成功地迁移并渗入到一种被称为胶质母细胞瘤(GBM)的致命脑部肿瘤。
该研究是由宾夕法尼亚大学的研究人员负责进行的一项首例人体试验,针对胶质母细胞瘤(GBM)的CAR-T疗法成功地跨越了血脑屏障到达脑部的肿瘤,同时也显示出了该疗法的安全性,并且在GBM细胞中,其表皮生长因子变体III(EGFRvIII)肿瘤靶标的水平显著降低。除此之外,该研究还发现,患者中EGFRvIII表达的广泛变化,再加上CAR-T细胞输注时引起的肿瘤免疫抑制效应被激活,这些可能是实体瘤临床应用方面代表性的障碍。
该研究小组由首席研究员Donald M. O'Rourke博士(宾夕法尼亚州神经外科副教授)和Marcela Maus博士共同领导,结果表明CART-EGFRvIII细胞具有可接受的安全性,可以跨越血脑屏障,浸润肿瘤,并且能够引起免疫应答,从而使得GBM细胞中EGFRvIII肿瘤抗原的减少。
肝癌:Eureka公司的AFP-CAR T
2017年6月,Eureka和合作伙伴MSKCC(MemorialSloan Kettering Cancer Center,纪念斯隆凯特琳癌症中心)共同在《Clinical Investigation》杂志上上发表了一项研究,表明其TCR-mimicking(TCRm)抗体可以识别和杀死小鼠模型内表达肿瘤胞内抗原PRAME的癌细胞。(注:Eureka研发的针对胞内抗原 peptide/MHC复合体靶点的治疗性抗体,在业界也被称为TCR-mimicking抗体,TCRm抗体或TCR样抗体)
虽然大多数以胞内抗原为靶点的方法都涉及到可穿透细胞的化合物,但是TCRm是从细胞外部起作用。其技术原理概括如下:Eureka专有抗体技术开发平台通过靶向MHC/免疫肽段复合物来发现识别肿瘤细胞内的特异性抗原。这些抗体因而能有效识别癌细胞内的特异蛋白质,然后调动免疫系统攻击相关肿瘤细胞。
随后,优瑞科生物技术公司与位于美国南加州的世界著名癌症研究和治疗中心City of Hope (以下简称希望之城) 达成协议, 开展一项名为ET1402L1-CAR的开放标签,剂量爬坡的嵌合抗原受体T细胞免疫疗法(CAR-T)临床一期试验。这项CAR-T疗法针对的是作为肝癌主要类型的肝细胞癌(hepatocellularcarcinoma, HCC)。ET1402L1是从优瑞科专有的E-ALPHA™ 噬菌体展示平台筛选出来的人源抗体,该抗体选择性地靶向甲胎蛋白(alpha-fetoprotein, AFP)高表达的肝癌细胞。
5 结语
CAR-T细胞疗法在血液肿瘤中大放异彩,让全球的癌症研究者纷纷投入到新技术的研发中,特别针对实体肿瘤来说,需要突破的地方还有很多。如何应对实体瘤面临的挑战,如何在特定的实体瘤上应用新的技术,例如本文提到的微导管技术,将成为CAR-T细胞疗法下半场竞争的焦点。我们希望有更多的实体瘤临床进展,医麦客也会持续的跟踪报道实体瘤CAR-T的最新进展,欢迎本领域的科学家,学者和同行给我们提供最新的素材资料。祝大家国庆中秋双节快乐。
参考出处:
http://ir.atossagenetics.com/press-releases/detail/824/atossa-genetics-announces-chimeric-antigen-receptor
http://html.rhhz.net/ZGZLLC/html/2017-9-2.htm(韩为东等“CAR-T细胞治疗实体瘤的挑战与思考”)
http://www.medscape.com/viewarticle/846702#vp_2
http://www.pressreleasepoint.com/celyad-announces-registration-first-pancreatic-cancer-patient-its-car-t-nkr-2think-trial-belgium
http://www.curetoday.com/publications/cure/2017/gi-special-issue/car-t-cell-therapy-being-tested-in-pancreatic-cancer?p=2
http://www.businesswire.com/news/home/20170607005051/en/Eureka-Therapeutics-City-Hope-Announce-Agreement-Conduct
医麦客 丨出品
中国生物医药产业新媒体
转载请联系:[email protected]
申明:文中资讯内容和事件评述仅代表作者观点,如果出现与事实不符或版权侵犯的内容,请速与医麦客平台联系,我们会尽快做出处理,欢迎更多读者朋友关注并给出指导建议。