「一周资讯」第46期,血糖控制不佳,还会影响认知功能?胖子的小心思居然那么容易就被看穿?
作者丨鲸鱼
来源丨医学界内分泌频道
本周提要:
■ 血糖控制差?长期认知能力可能下降!
■ 饱了还想吃?人胖了脑子还真不一样!
■ 慢病不控制?八种标志物与癌症相关!
血糖控制差?长期认知能力可能下降!
DOI:10.1007/s00125-017-4541-7.
已有的纵向追踪研究和临床试验提示,糖尿病患者的痴呆风险较常人要高,那么糖尿病是否会和认知水平相关呢?最近发表在Diabetologia上的研究提示,糖尿病或糖尿病前期,HbA1c水平较高与长期认知水平的下降有关,也就是说:血糖没控制好,人可能就傻了!
这项研究纳入了5189名英国老龄化追踪研究(English Longitudinal Study of Ageing, ELSA)的参与者,平均年龄65.6 ± 9.4岁,基线HbA1c水平在3.6%~13.7%之间,平均随访时间8.1 ± 2.8年。随访期间,研究人员通过让参与者回忆是个不相关的单词的方法检测他们的记忆力,通过让他们在一分钟内说出尽可能多的动物名字的方法检测了他们的执行力。在两项测试中获得的分数越高,说明他们的认知能力越好,基线认知能力评分为4.9 ± 1.5分。
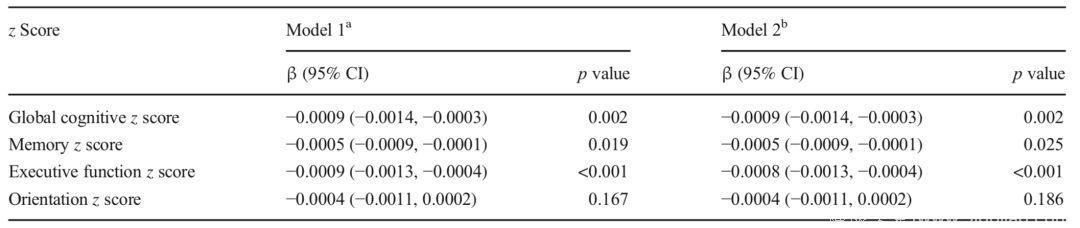
Fig 1.1 HbA1c水平升高与认知能力下降有关
结果发现,在调整了年龄、性别、总胆固醇、甘油三酯、高敏C反应蛋白、教育程度、吸烟、饮酒等17种因素之后,HbA1c水平的升高与参与者的认知评分、记忆评分以及执行评分下降显著相关,HbA1水平每上升1 mmol/mol,其认知评分每年改变−0.0009 SD(95% CI −0.0014~−0.0003) ,记忆评分每年改变−0.0005 SD( 95% CI −0.0009~−0.0001),执行评分每年改变−0.0008 SD(95% CI −0.0013~−0.0004)。
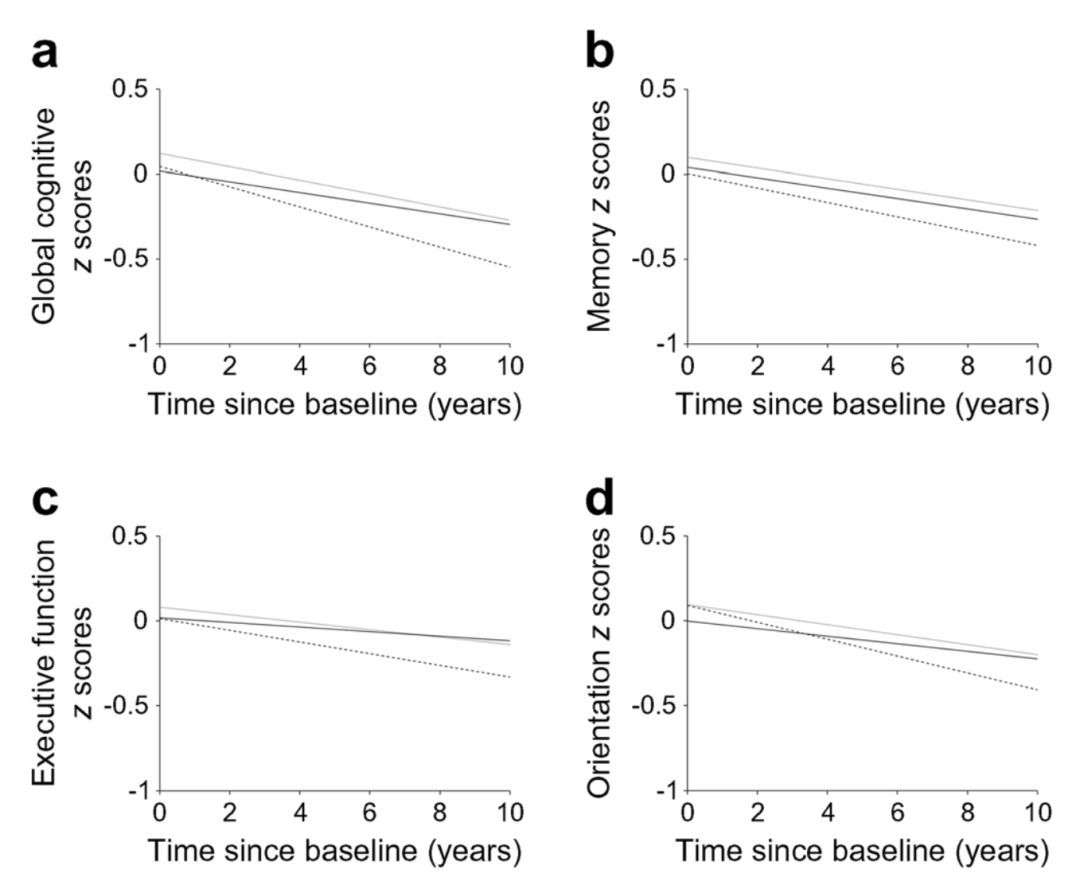
Fig 1.2 糖尿病患者的认知能力下降较正常人更甚(实线:正常;灰线:糖尿病前期;虚线:糖尿病)
而与血糖正常的参与者相比,糖尿病前期或患糖尿病的参与者认知功能的下降更为严重(p for trend <0.001),分别达到了每年改变-0.012 SD(95% CI −0.022~−0.002)和−0.031 SD(95% CI −0.046~−0.015),其记忆力、执行力等的下降也更为严重。
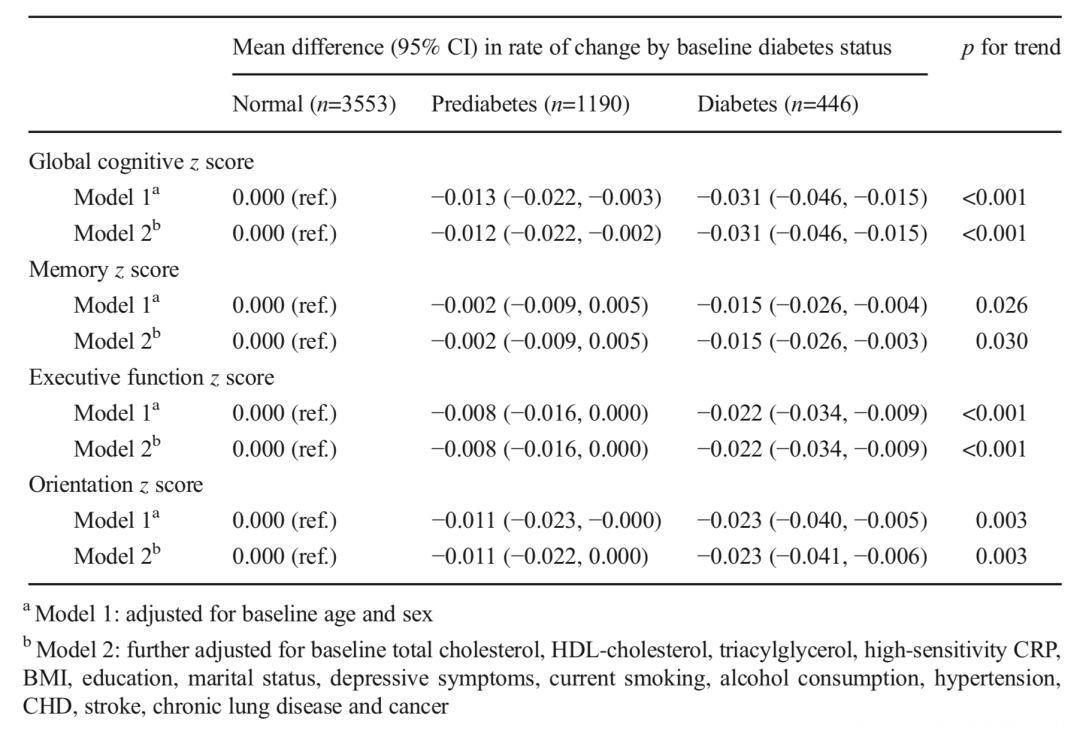
Fig 1.3 糖尿病及糖尿病前期均与认知能力下降有关
由此可见,糖尿病不仅和痴呆风险增加相关,甚至还会影响认知功能,对于HbA1c控制不佳、水平较高的患者更是敲响了警钟。
REF:Fanfan Zheng, Li Yan, Zhenchun Yang, Baoliang Zhong, Wuxiang Xie. (2018). HbA1c, diabetes and cognitive decline: the English Longitudinal Study of Ageing. Diabetologia, published online 25 Jan 2018. doi:10.1007/s00125-017-4541-7.
饱了还想吃?人胖了脑子还真不一样!
DOI:10.1152/ajpendo.00335.2017.
人体的血糖水平能够影响食物的摄入,以维持人体能量的平衡。如果吃得多、动得少,那么就很容易摄入过多的能量,人也就胖了。而最近发表在AJPEM上的研究则发现,在肥胖的人群中这一调节机制可能有所不同,即使在血糖较高的时候,大脑依然不能抵御食物的诱惑,俗称:饱了还想吃!
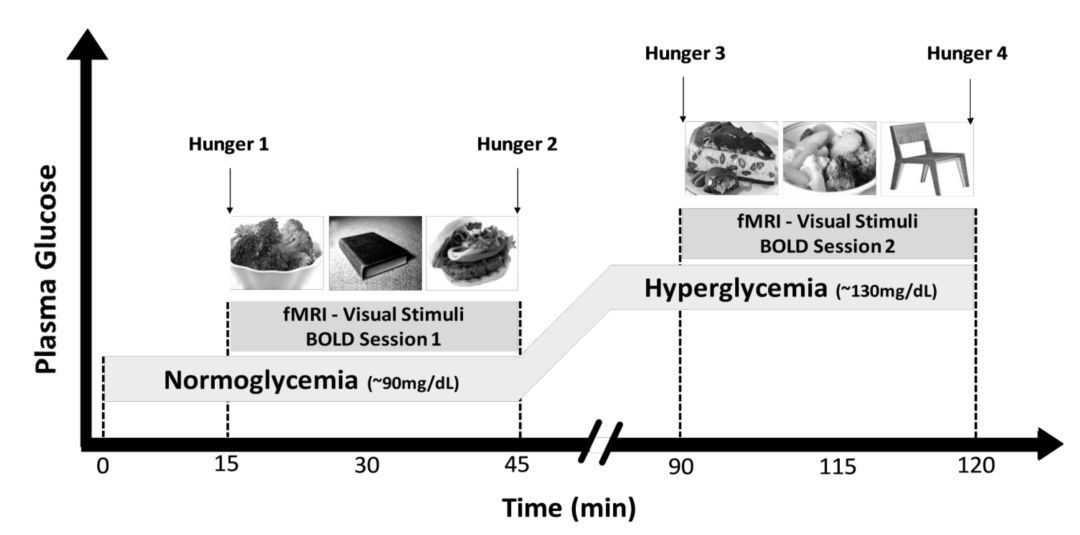
Fig 2.1 分别在正常/高血糖时,进行fMRI检查
研究人员选择了10名肥胖的成年人以及10名没有糖尿病的健康成年人参与研究(34±3 vs 23±2 kg/m2, p<0.0001)。在血糖正常(~95 mg/dL)以及高血糖(~130 mg/dL)的情况下,研究人员分别向他们展示了食物和非食物的图片,同时他们进行了大脑功能磁共振检查(functional MRI, fMRI)并测定了血液中的胰岛素、瘦素(leptin)和饥饿激素(ghrelin)的水平。
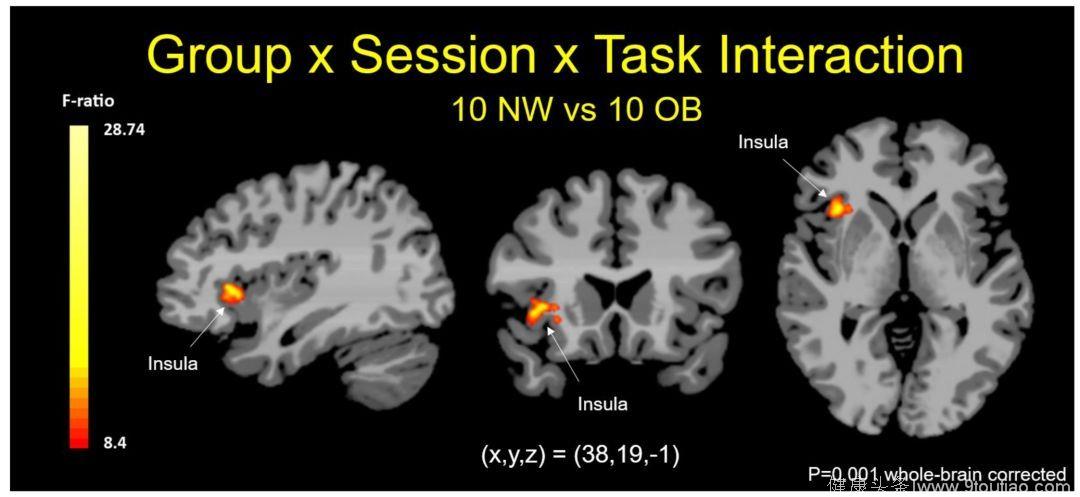
Fig 2.2 肥胖与正常人群面对食物时岛叶的活动度不同
结果发现,肥胖人群胰岛素和瘦素的水平较体重正常人群高,而饥饿激素水平则较低(P均<0.05)。而fMRI的结果显示,与血糖水平正常时相比,非糖尿病的健康人在血糖水平时较高时,其下丘脑和纹状体豆状核壳对于食物图片的反应活动度更低(P<0.001);然而,肥胖人群在血糖水平较高时,其大脑岛叶、纹状体豆状核壳、前额叶及背外侧额叶皮层(aPFC/dLPFC)均显示出活动度的增高(P<0.001)。
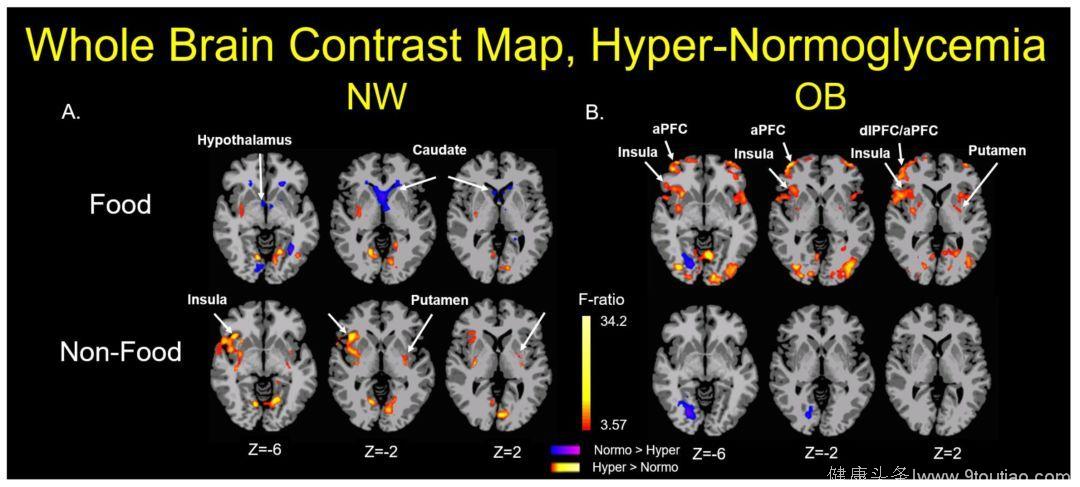
Fig 2.3 肥胖人群看到食物更加“难以自持”
这一研究提示,在正常情况下,高血糖时人体对于食物应该不那么感兴趣,在正常人中表现为岛叶的活动度减低,但这一现象在肥胖人群中却消失了,甚至岛叶的活动度还会增加,而这一区域正与对食物的感知相关。同时,肥胖人群的的纹状体以及额叶皮层的活动度增加则可能分别与摄食活动的失调和不良的自我控制有关。
万万没想到,饱了还想吃的小心思,就这样被看穿了……
REF:Renata Belfort-DeAguiar, Dongju Seo, Cheryl Lacadie, Sarita Naik, Christian Schmidt, & Robert S. Sherwin, et al. (2018). Obese Humans Have Disordered Brain Responses to Food Images During Physiological Hyperglycemia. American Journal of Physiology-Endocrinology and Metabolism, published online 30 Jan 2018. doi:10.1152/ajpendo.00335.2017.
慢病不控制?八种标志物与癌症相关!
DOI:10.1136/bmj.k134.
我们都知道年龄的增加和各种不健康的生活方式都可能与癌症风险相关,但却没有研究涉及各种慢性疾病与癌症的关系。而近日发表于BMJ的一项来自宝岛台湾的研究就关注到了这样的一个问题,发现了八种与癌症风险相关的慢性病或标志物。
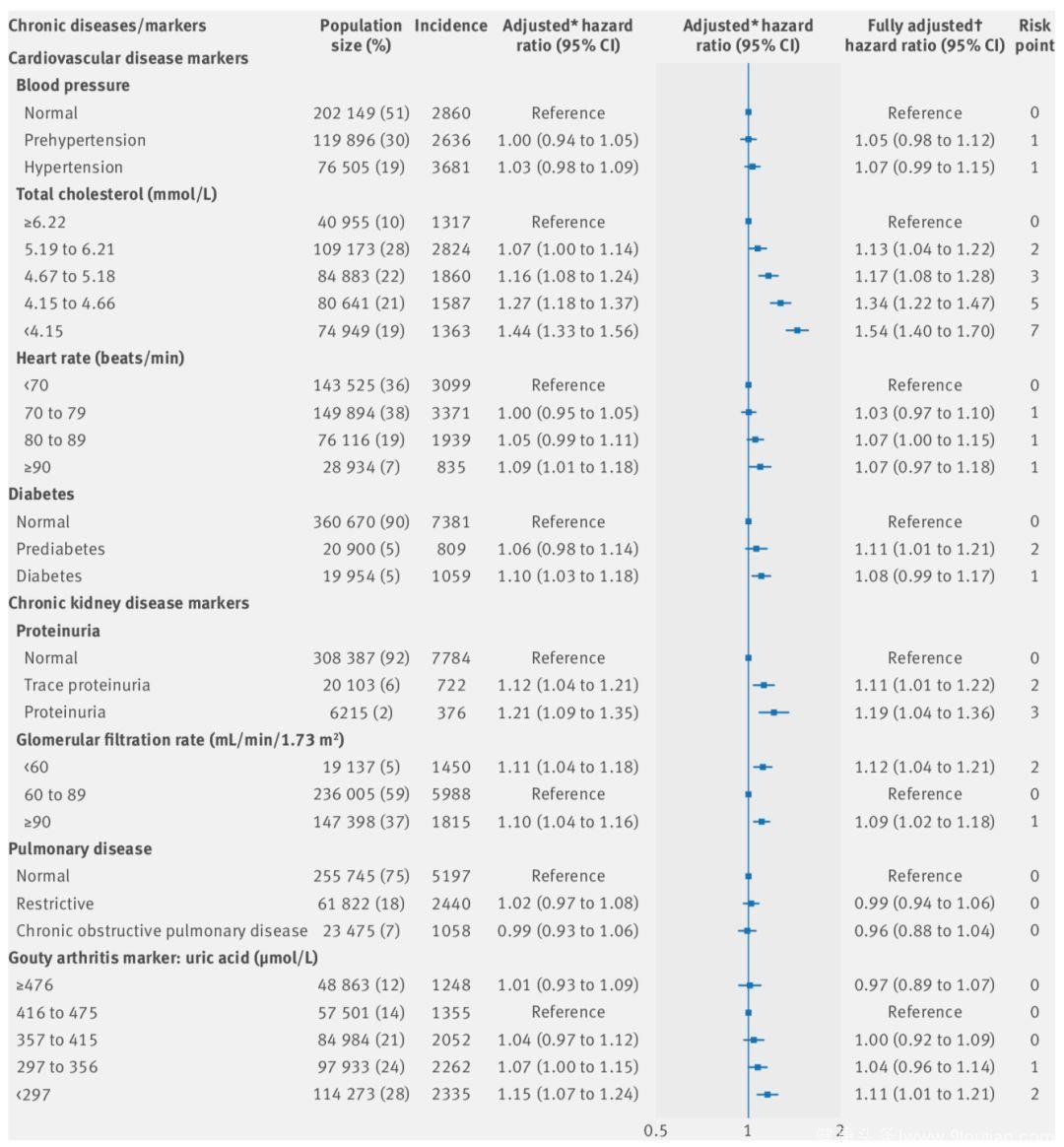
Fig 3.1 慢性疾病标志物与癌症发病风险相关
这项研究纳入了405878名参与者,平均随访时间8.7年。研究人员测定了参与者的血压、总胆固醇、心率等心血管疾病标志物,蛋白尿、肾小球滤过率等慢性肾病标志物以及糖尿病、肺部疾病、痛风等疾病的患病情况;同时,还对参与者的运动量进行了分类,研究这些因素与癌症风险的关系。

Fig 3.2 慢性疾病标志物与癌症死亡风险相关
结果发现,除了血压和肺部疾病,这些慢性疾病或标志物均与癌症发病风险增加相关,调整后风险比在1.07倍~1.44倍不等;同时,这八种慢性疾病或标志物与癌症的死亡风险增加同样相关,调整后的风险比在1.12倍~1.70倍不等。
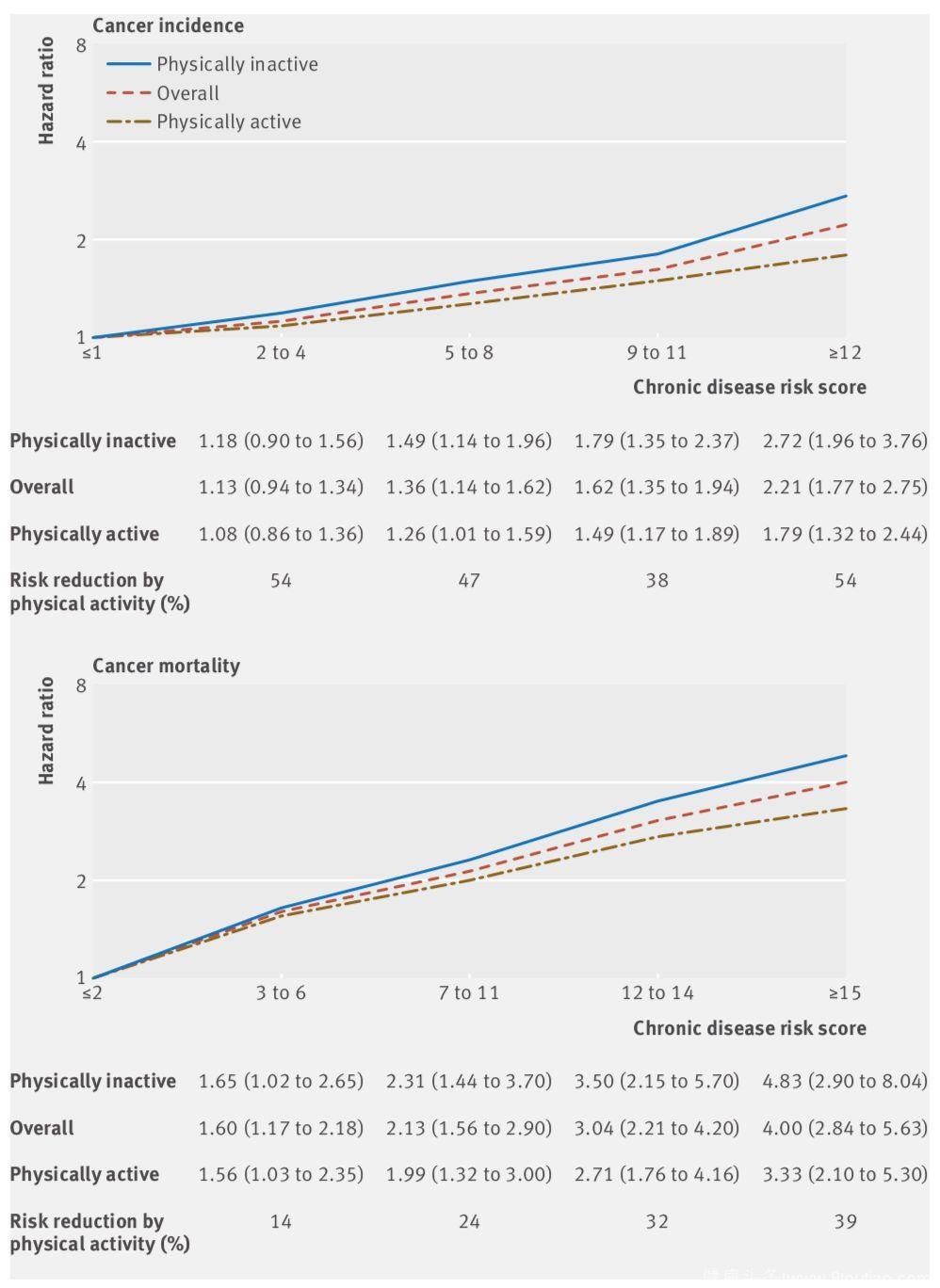
Fig 3.3 慢病评分越高癌症风险也越高
剂量-反应分析显示,综合了这八种慢性疾病或标志物的慢病评分与癌症风险正相关,其癌症患病及死亡风险最高可增加2.21倍(95% CI 1.17~2.75)和4.0倍(95% CI 2.84~5.63),这些风险对慢病患者生存时间的威胁也很大,男性最多会降低13.3年,女性更高达15.9年。
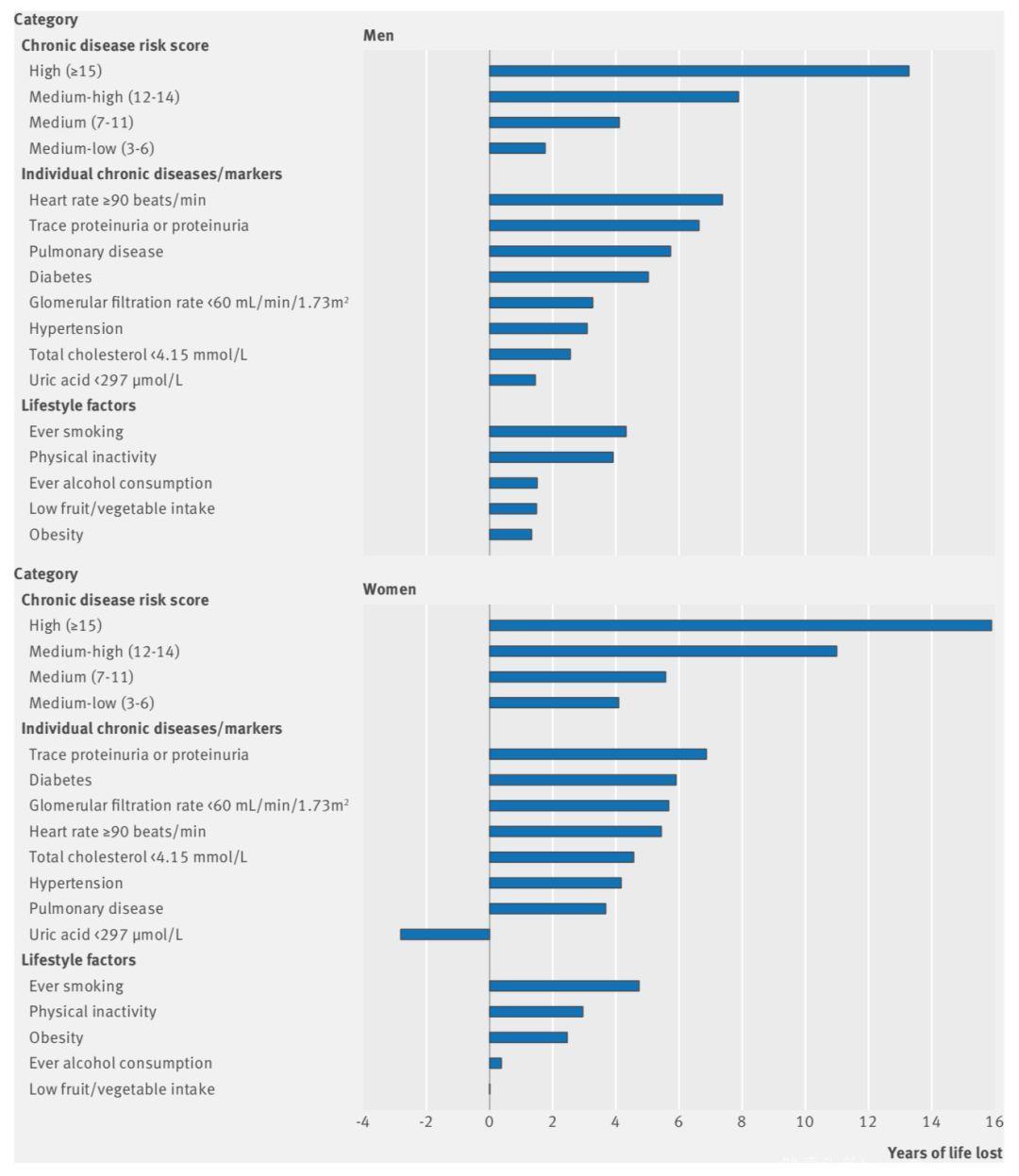
Fig 3.4 八种慢性疾病标志物影响生存时间
这八个慢性疾病或标志物对于癌症发病风险的归因系数百分比接近于不良的生活方式(20.5% vs 24.8%),对于癌症死亡的归因系数百分比甚至与之相当(38.9% vs 39.7%)。那么,面对这些癌症风险我们难道就束手无策了吗?当然不是!这项研究最后给我们带了了一些希望——运动能够降低与慢病相关的48%的癌症发病和27%的癌症死亡风险!
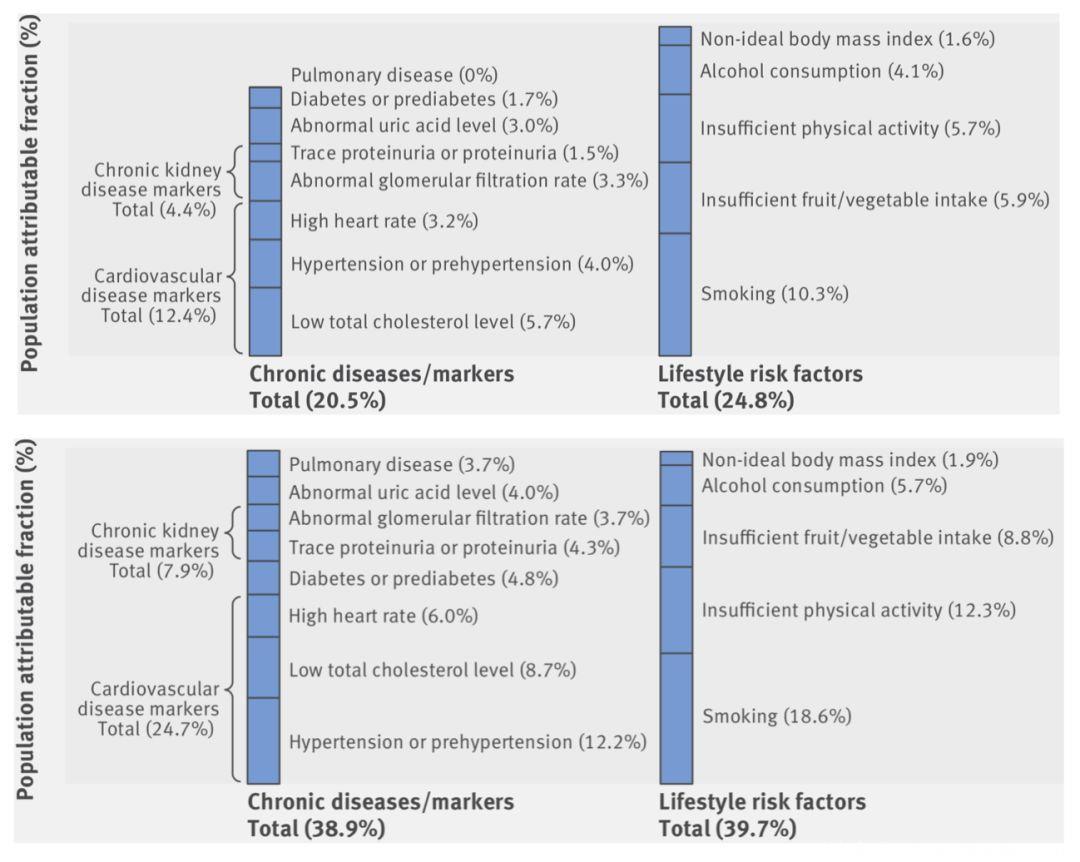
Fig 3.5 慢病标志物对癌症风险的影响与生活方式相当
话不多说,我写完稿就要赶紧出门走走!
REF:Huakang Tu, Chi Pang Wen, Shan Pou Tsaii, Wong-Ho Chow, Christopher Wen, & Xifeng Wu et al. (2018). Cancer risk associated with chronic diseases and disease markers: prospective cohort study. BMJ 2018;360:k134, published online 31 Jan 2018. doi: 10.1136/bmj.k134.
「一周资讯」系列,点击蓝字即可查看往期内容: