艾伯维(AbbVie)与 Neurocrine Biosciences 今日宣布,子宫肌瘤在研新药 elagolix 的 3 期临床研究 ELARIS UF-II(M12-817)达到了主要终点。本次研究是另外一项关键 3 期试验 ELARIS UF-I(M12-815)的重复性试验,其研究结果已于 2018 年 2 月公开。此次研究证实了第一项试验的结果,显著减少了子宫肌瘤患者的重度月经出血,达到了研究的主要终点。

子宫肌瘤,也称为平滑肌瘤或肌瘤,是非癌性,激素反应性子宫肌肉组织肿瘤。子宫肌瘤是女性骨盆中最常见的异常生长,可影响约 20-80% 的 50 岁以下的女性。肌瘤的大小,形状,数量和部位不等。子宫肌瘤患者可能无症状,但在某些女性中,肌瘤可引起严重的月经出血、痛经、乃至怀孕困难等严重问题。
Elagolix 是一种促性腺激素释放激素(GnRH)受体拮抗剂,是一种口服的短效分子,通过与脑垂体中的 GnRH 受体竞争结合来阻断内源性 GnRH 信号。在治疗中进行快速可逆和剂量依赖性的抑制黄体生成素(LH)和卵泡刺激素(FSH)分泌,可导致卵巢性激素,雌二醇和孕酮的生成减少。Elagolix 目前正在卵巢性激素介导疾病,如子宫肌瘤和子宫内膜异位症患者中进行研究。迄今为止 Elagolix 已在超过 40 项临床试验中进行了研究,共计超过 3700 名受试者。
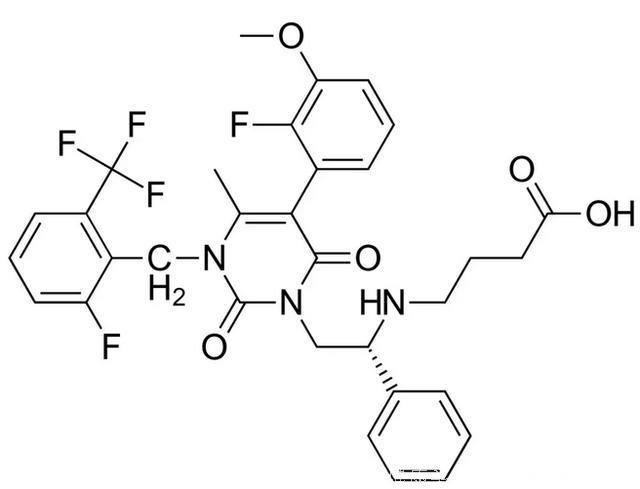
Elagolix 的分子结构式(图片来源:By Vaccinationist (PubChem) [Public domain or Public domain], via Wikimedia Commons)
ELARIS UF-II 是两项为期 6 个月的重复 3 期临床试验的第二项,评估单独使用 elagolix 和 elagolix 联合低剂量激素疗法(雌二醇 / 醋酸炔诺酮)的安全性,耐受性和疗效。研究对象为 18 至 51 岁经阴道和经腹部盆腔超声检查(TVU)诊断为子宫肌瘤的绝经前妇女。主要终点为通过碱性血红素法测量,评估患者重度月经出血减少。临床缓解被定义为在第 6 个月时月经失血量少于 80 毫升,并且经血失血量从基线至第 6 个月减少至少 50%。次要终点包括出血,出血抑制和血红蛋白变化。该研究在美国和加拿大的约 100 个地点进行。
本次试验结果显示,研究第 6 个月时,每日服用两次 300 毫克 elagolix 联合低剂量激素疗法(雌二醇 1.0 毫克 / 醋酸炔诺酮 0.5 毫克),可帮助 76.2%(p <0.001)的子宫肌瘤妇女患者减少重度月经出血,达到临床缓解。Elagolix 的总体安全性曲线与子宫肌瘤 2 期临床试验和第一个 3 期临床试验(ELARIS UF-I)中观察到的一致。来自 ELARIS UF-II 的 3 期研究数据将支持提交 elagolix 的监管审查。研究人员将在这项正在进行的研究中,持续收集安全性数据,包括观察最常见的不良事件。此次 6 个月的主要分析结果与 2018 年 2 月报告的 ELARIS UF- I 研究结果一致,并将在即将召开的医疗会议上公开。研究中的女性患者将继续进行治疗后随访,或六个月的盲法延长研究。
“目前诊断患为子宫肌瘤的数百万妇女所面临的非手术选择有限,”AbbVie 普通药物开发副总裁 Dawn Carlson 博士说:“这项研究的结果表明,elagolix 有可能成为患有子宫肌瘤的女性的重要口服治疗选择。”
我们期待这款重要子宫肌瘤新药能够顺利通过监管审查,早日为广大女性患者减少痛苦,带来康复。
参考资料:
[1] AbbVie’s Elagolix Dazzles in Phase III Trial
[2] AbbVie Announces Positive Topline Results from Second Phase 3 Study Evaluating Investigational Elagolix in Women with Uterine Fibroids
[3] 药明康德 - 艾伯维子宫肌瘤新药 3 期临床试验数据积极











